Co-factor schakelt katalysator
16 January 2019
De chemie van de natuur is bijzonder efficiënt en vernuftig. In een cel, een complex mengsel van stoffen, zorgen enzymen precies op het juiste moment voor de omzetting van precies de juiste stoffen. Om deze natuurlijke katalyse goed te laten verlopen, gebruikt een cel kleine signaalmoleculen en 'cofactoren' die de werking van het enzym reguleren.
Ook bij synthetisch chemische processen, bijvoorbeeld voor de productie van farmaceutische moleculen, is in toenemende mate sprake van complexe mengsels. Dat heeft onder andere te maken met de omschakeling naar hernieuwbare, duurzame grondstoffen uit biomassa. Waar huidige petrochemische grondstoffen (uit olie) vaak een redelijk homogene samenstelling hebben, zijn in 'groene' grondstoffen veel meer verschillende moleculen te vinden. Dit maakt het van belang om precies op het juiste moment van het syntheseproces de katalysator zijn werk te laten doen, onder andere om te voorkomen dat er ongewenste bijproducten ontstaan. Maar in de homogene katalyse, waarbij de katalysator - net als een enzym - is opgelost in het reactiemedium, is dat 'aanzetten' van de katalysator makkelijker gezegd dan gedaan.
Capsule
Bij de onderzoeksgroep 'Homogeneous, Supramolecular and Bio-inspired Catalysis' van hoogleraar Joost Reek kijken onderzoekers bij de ontwikkeling van nieuwe homogene katalysatoren al langer naar de werking van enzymen. Promovendus Lukas Jongkind ontwikkelde samen met chemici van de Radboud Universiteit Nijmegen de nieuwe katalysator die met behulp van een kleine cofactor is aan te zetten, en waarvan de werking bovendien heel selectief is.
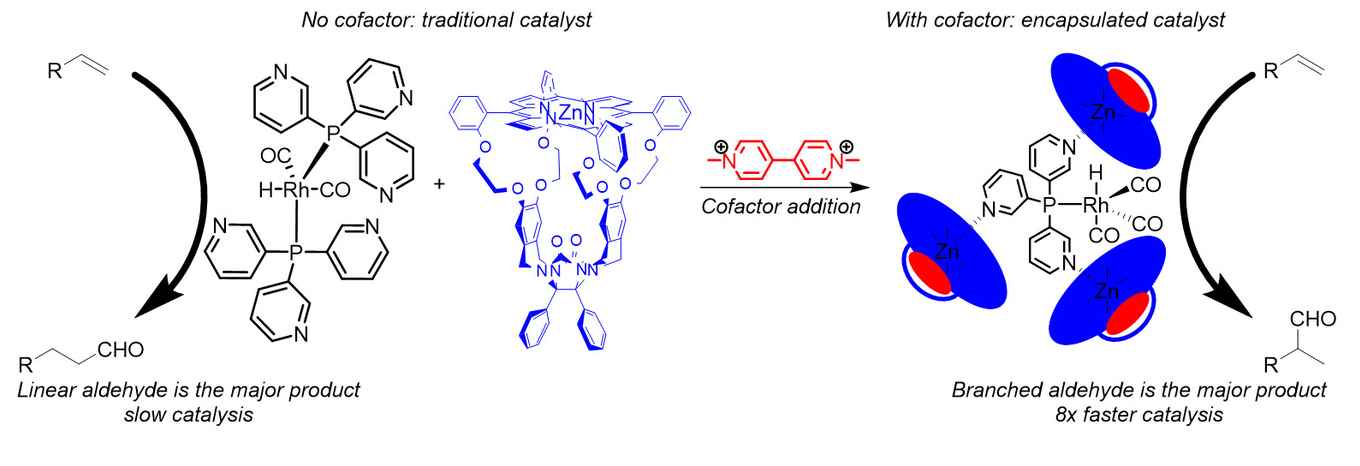
De katalysator bestaat uit supramoleculaire bouwstenen waarvan de onderlinge interacties gereguleerd kunnen worden. Zonder cofactor hebben de bouwstenen geen interactie met elkaar en is er slechts sprake van inefficiënte katalyse. Pas als de cofactor wordt toegevoegd vormen zeven bouwstenen vanzelf een capsule om een katalytisch actief rhodium atoom, dat eveneens in de oplossing aanwezig is. De capsule lijkt qua vorm en functie op de structuren die bij enzymen aanwezig zijn rond de 'active site' en daar een belangrijke rol spelen bij het verloop van selectieve reacties.
Lukas Jongkind onderzocht de werking van de katalysator in rhodium gekatalyseerde hydroformylering, een proces waarbij alkenen worden omgezet in aldehydes. Dat is een van grootste industriële toepassingen van homogene katalysatoren. De regulatie met de cofactor blijkt hier bijzonder goed te werken: na toevoeging van de cofactor resulteert de vorming van de capsule in een achtvoudige versnelling van de hydroformylering. Bovendien ontstaat dan een ander aldehyde dan in afwezigheid van de cofactor. De capsule introduceert dus een nieuwe selectiviteit bij de hydroformuleringsreactie.
Nieuwe katalysatoren
Met deze resultaten hebben de onderzoekers laten zien dat het mogelijk is relatief simpele homogene katalysatoren te reguleren op een manier die lijkt op de regulatie bij complexe enzymen. Dit biedt mogelijkheden voor de ontwikkeling van nieuwe homogene katalysatoren die selectief te werk kunnen gaan in complexe mengsels van stoffen.